혁신적인 약물은 여러 치료 영역과 임상 발달에 들어가는 후보와 관련된 비용, 시간 및 위험이 크게 증가합니다. 합리적인 연구 전략을 사용하고, 기존 기술을 최대한 활용하고, 개발 잠재력을 가진 후보자에게 자원을 집중시키고, 성공할 수없는 프로젝트에서 자원 폐기물을 최소화하기 위해 실행 가능한 미래가없는 사람들을 제거해야합니다.
임상 발달 위험을 완화하고 성공률을 높이며 안전하고 효과적인 약물의 승인을 가속화하는 방법에 대한 간단하고 기성품 답변은 없습니다. 또한, 연구 전략은 치료 분야에 따라 크게 다릅니다. 가장 칭찬 된 접근법 중 하나는 초기 단계 연구에서 기계 및 개념 증명 (POC) 검증을 사용하는 것입니다. 2024 "아데노 관련 바이러스 (AAV) 벡터 유전자 요법 제품의 비 임상 연구에 대한 지침도 POC의 중요성을 명시 적으로 언급합니다. 그러나 POC를 통해 정확히 검증되는 것은 무엇입니까?
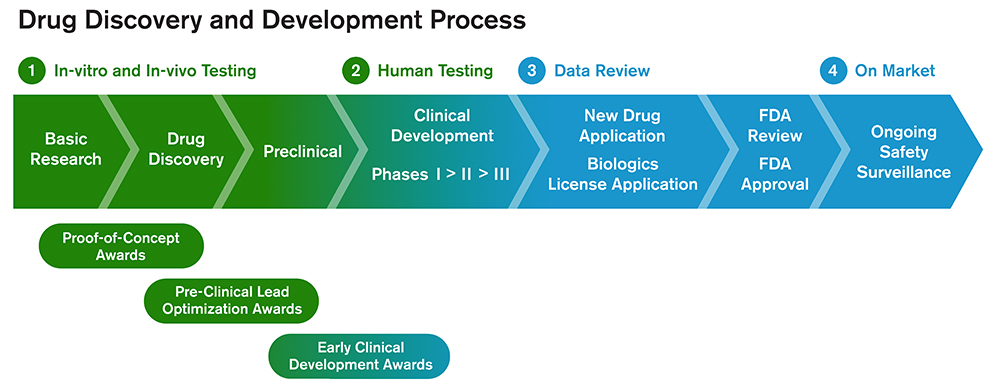
유전자 요법은 질병 메커니즘에 대한 깊은 이해를 기반으로 설계되었으며, 표적 조직 또는 세포에서 효과적으로 표현하고, 표적 부위에 결합하고, 질병 진행을 변화시키고 임상 적 이점을 초래하는 약리학 적 효과를 발휘하기 위해 그들의 기능을 조절하기 위해 개발된다. 표적 외 효과는 불리한 것으로 간주됩니다. 과정은 다음 단계에서 간단히 설명 할 수 있습니다. ② 약물은 표적 세포를 발현하고 표적 부위에 결합한다. target 목표 부위는 약리학 적 효과를 유발합니다. ④이 효과는 임상 적으로 유의 한 변화를 가져옵니다 (치료 결과).
개발 초기에 약물의 작용 메커니즘을 이해하면 약물 설계 및 최적화를 안내하여 추가 개발을위한 최상의 후보를 선택할 수 있습니다. 이후 단계에서는 행동 메커니즘을 검증하기 위해 방법을 사용하여 지속적인 개발을위한 토대를 마련하고 궁극적으로 성공률을 높이고 위험을 줄입니다.
전임상 개념 증명 (POC)포함됩니다시험 관내및 효능 및 예비 안전 평가를 포함하여 AAV 기반 치료 전략이 실현 가능한지 여부를 처음으로 확인하는 동물 연구. 실험실 연구에서 전임상 발달로의 중요한 전환 (GLP 독성학 연구).
POC의 핵심 목표
- 과학적 가설 검증: AAV 벡터가 표적 조직에서 표현되는지 여부 및 질병 표현형을 개선 할 수 있는지 여부를 대상 유전자를 전달할 수 있는지 여부를 확인합니다.
- 위험 관리: 나중에 개발 중에 고장 위험을 최소화하기 위해 잠재적 문제 (예 : 면역 원성, 표적 외 효과)를 식별합니다.
- 최적화: 최적의 벡터 설계 (혈청 형, 프로모터), 투여 경로 및 용량 범위를 결정합니다.
POC가 필요한 이유는 무엇입니까?
- 과학적 검증: 유전자 편집/대체 전략이 살아있는 모델에 효과적이며 세포 기반 실험에서 볼 수있는 오 탐지를 피하십시오. AAV의 조직 표적화가 기대치와 일치한다는 것을 확인하십시오 (예 : AAV9의 혈액 뇌 장벽을 가로 지르는 능력).
- 개발 위험 감소: 약물 발달 실패의 약 70%는 전임상 단계에서 불충분 한 효능 또는 독성 문제에서 비롯됩니다 (자연 검토 약물 발견). POC는 비효율적 인 전략을 조기에 선별하는 데 도움이됩니다.
- IND 응용 프로그램 지원: POC 데이터는 규제 기관 (예 : FDA, EMA)에 대한 핵심 참조입니다. 임상 시험의 이론적 근거를 평가합니다. POC가 부족하면 Ind가 거부 될 수 있습니다.
- 투자 유치: 명확한 POC 결과는 특히 고가의 유전자 요법 분야에서 자금 조달 및 파트너십의 기초를 제공합니다.

POC를 구현하는 방법?
목표 선택 및 질병 모델
질병 메커니즘: 단일 유전자 장애 (예 : 혈우병) 또는 다 인성 질환 (예 : 신경 퇴행성 질환)인지 이해하십시오.
녹아웃/돌연변이 모델 (예 :류마티스 관절염/CIA).
유도 된 모델 (예 :간 지방증/ 내쉬/ 매쉬).
모델 병리학의 검증과 인간 질병에 대한 유사성의 검증이 필수적입니다.
AAV 벡터 설계
- 혈청 형 선택: 표적 조직을 기준으로 선택하십시오 (예 : AAV8은 간을 대상으로, CNS 용 AAVRH10).
- 프로모터 최적화: 조직 특이 적 프로모터 (예 : 심근의 CTNT)를 사용하여 표적화 된 발현을 향상시킵니다.
- 트랜스 진 디자인: 코돈 최적화 및 조절 요소 (예 : 향상된 발현을위한 WPRE)를 포함합니다.
시험 관내 연구
- 셀 라인 검증: HEK293 세포 또는 1 차 세포에서 벡터 형질 도입 효율, 유전자 발현 수준 및 독성을 시험한다.
- 표적 외 분석: RNA-Seq 또는 전체 게놈 시퀀싱을 통해 의도하지 않은 편집을 평가합니다.
- 생체 내 작은 동물 연구
- 관리 경로: 정맥 내 (전신 전달), 국소화 (해당) 또는 뇌내 주사.
효능 마커
바이오 마커 (예 : 응고 인자 IX 활동의 증가).
기능적 회복 (예 : 근력 검사, 행동 개선).
조직 학적 분석 (예 : 표적 단백질 발현에 대한 면역 조직 화학).
복용량 탐사
다양한 용량을 테스트하여 최소 유효 용량 (MED) 및 최대 내약성 용량 (MTD)을 결정합니다.
예비 안전 평가
- 급성 독성:무게, 활동 및 혈청 생화학 마커 (예 : Alt/AST)를 모니터링합니다.
- 면역 원성: AAV 및 T- 세포 반응에 대한 중화 항체를 평가합니다 (예 : ELISPOT에 의한 IFN- 분비).
- 벡터 분포: QPCR을 사용하여 주요 기관 (간, 심장, 뇌, 생식선)에서 벡터 DNA를 평가하십시오.
장기 후속 조치
유전자 발현 지속성 (6-12 달) 및 시간이 지남에 따라 잠재적 인 감소를 모니터링합니다.
지연 독성을 찾으십시오 (예 : 간 섬유증, 종양 형성 위험).
전임상 연구를위한 표준 지원
Cohen의 출판 된 연구는 후보 약물의 발전을 지원하는 세 가지 주요 기둥을 요약합니다.
- 목표 노출: 약물은 목표 부위에 도달해야합니다.
- 목표 점유: 약물은 목표에 효과적으로 결합해야합니다.
- 기능적 행동: 약물은 목표물에서 기능적 효과를 유발해야합니다.
이 세 가지 기준이 충족되면 성공적인 약물 개발 가능성이 가장 높습니다. 그들 중 일부 만 충족되거나 충족되지 않으면 성공 가능성이 상당히 줄어 듭니다. AAV 유전자 요법 제품의 경우 이러한 기준의 추가 개선이 필요합니다.
주요 성공 요인
1 차 효능 종점에서의 현저한 개선 (예 : 질병 관련 단백질 발현이 정상의 20% 이상 또는 동일).
효능의 복제는 적어도 두 가지 모델 (예 : 생쥐 + 큰 동물)을 초래합니다.
수용 가능한 안전
심각한 독성 (예 : 간부전, 신경 염증).
제어 가능한 면역 반응 (중화 항체 역가<1:100 or manageable with immunosuppressive pretreatment).
명확한 복용량 범위
MED 및 MTD를 확립하고 용량-반응 관계를 정의하십시오.
명확한 행동 메커니즘
표적 조직에서 AAV 벡터 생체 분포 및 트랜스 진 발현을 확인합니다 (예 : 생체 내 영상 또는 조직 섹션을 사용하여).
재현성과 안정성
Independent production of AAV vectors in different batches, with consistent results and compliance with preliminary quality control standards (e.g., purity >90%, 빈 캡시드 속도<20%).
고려 사항
동물 모델의 한계
설치류 모델은 인간 질병 (예 : 면역계 차이)을 완전히 복제하지 않을 수 있으며, 큰 동물 (돼지,NHPS).
규제 변형
FDA 지침 (예 : 2020 "신경 퇴행성 질환에 대한 인간 유전자 요법")은 특정 안전 데이터 (예 : 생식 독성)를 필요로 할 수 있습니다.
자원 평가
POC 단계에서, 연구 깊이의 균형이 비용과 균형을 잡는 것이 중요합니다 (예 : 트랜스 제닉 마우스 사용은 유도 된 모델보다 더 비쌀 수 있습니다).
결론
전임상 POC는 AAV 유전자 요법 개발의 핵심 구성 요소이며, 치료 파라미터를 최적화하면서 효능 및 안전성의 체계적인 검증이 필요합니다. 성공 기준에는 재현 가능한 효능 데이터, 제어 가능한 독성 위험 및 명확한 용량-반응 관계가 포함되며, 궁극적으로 IND 응용 및 임상 시험의 기초를 마련합니다.












